氧化还原反应

【知识梳理】
1.双线桥理解基本概念
氧化性:氧化剂>氧化产物 还原性:还原剂>还原产物
2.多种方法判断强弱
(1)金属活动性顺序
(2)非金属活动性顺序
一般来说,元素非金属性越强,单质越易得到电子,氧化性越强;其对应阴离子越难失电子,还原性越
弱。
(3)依据元素周期律及周期表中元素性质变化规律来判断氧化性、还原性的强弱
同周期,从左至右,核电荷数递增,非金属性逐渐增强,金属性逐渐减弱,单质氧化性逐渐增强,还原
性逐渐减弱;
同主族,从上至下,核电荷数递增,非金属性逐渐减弱,金属性逐渐增强,单质氧化性逐渐减弱,还原
性逐渐增强。
(4)根据原电池的正负极来判断:
在原电池中,在负极反应的物质还原性一般比作正极物质的还原性强。
3.典型物质判断
(1)典型粒子氧化(或还原)性强弱:
氧化性:Br2>Fe3+>I2>S
还原性:S2->I->Fe2+>Br-
氧化性:Fe3+>Ag+>Cu2+>Fe2+>Zn2+>Al3+
(2)有单质参加的反应或有单质生成的反应不一定是氧化还原反应。如同素异形体之间的相互转化
(O2→O3)。
(3)金属阳离子被还原,不一定得到金属单质。如向 FeCl3溶液中加入少量 Zn,得到 Fe2+。
(4)向 FeBr2、FeI2的混合物中加入新制氯水,最先被氧化的是 I-。
(5)盐酸有酸性、氧化性、还原性;亚硫酸有酸性、氧化性、还原性、漂白性。
(6)Ca(ClO)2溶液中通 SO2、FeS+HNO3、Na2SO3+HNO3、Fe(OH)2+HNO3、Fe(OH)3+HI 发生氧化还原反应。
(7)氧化还原反应配平:标价态、列变化、求总数、定系数、后检查
一标:标出有变化的元素化合价;
二列:列出化合价升降变化;
三找:找出化合价升降的最小公倍数,使化合价升高和降低的数目相等;
四定:确定氧化剂、还原剂、氧化产物、还原产物的系数;
五平:观察配平其它物质的系数;
六查:检查是否原子守恒、电荷守恒(通常通过检查氧元素的原子数),画上等号。
(8)常见的重要氧化剂、还原剂
氧化剂 还原剂
活泼非金属单质:X2、O2、S 活泼金属单质:Na、Mg、Al、Zn、Fe
某些非金属单质: C、H2、S
高价金属离子:Fe3+、Sn4+
不活泼金属离子:Cu2+ 、 Ag+其它:
[Ag(NH3)2]OH、新制 Cu(OH)2
低价金属离子:Fe2+、Sn2+
非金属的阴离子及其化合物:
S2-、H2S、SO32- 、I -、HI、NH3、Cl-、HCl、Br-、HBr
含 氧 化 合 物 : 低 价 含 氧 化 合 物 :
第1页(共 24 页)
NO2、N2O5、MnO2、Na2O2、H2O2、HClO、HNO3、浓
H2SO4、NaClO、Ca(ClO)2、KClO3、KMnO4、王水
(浓盐酸:浓硝酸 3:1 混合成的酸)
CO、SO2、H2SO3、Na2SO3、Na2S2O3、NaNO2、H2C2O4、含-CHO 的有机物
(醛、甲酸、甲酸盐、甲酸某酯、葡萄糖、麦芽糖)等
既作氧化剂又作还原剂的有:S、SO32-、HSO3-、H2SO3、SO2、NO2-、Fe2+及含-CHO 的有机物。
【直击高考】
一.选择题(共 18 小题)
1.(2022•浙江)关于反应 Na2S2O3+H2SO4═Na2SO4+S↓+SO2↑+H2O,下列说法正确的是( )
A.H2SO4发生还原反应
B.Na2S2O3既是氧化剂又是还原剂
C.氧化产物与还原产物的物质的量之比为2:1
D.1molNa2S2O3发生反应,转移4mol 电子
2.(2023•福建)稀有气体氙的氟化物(XeFn)与NaOH 溶液反应剧烈,与水反应则较为温和,反应式
如下:
与水反应 与NaOH 溶液反应
i.2XeF2+2H2O═2Xe↑+O2↑+4HF ii.2XeF2+4OH﹣=2Xe↑+O2↑+4F﹣+2H2O
iii.XeF6+3H2O═XeO3+6HF iv.2XeF6+4Na++16OH﹣═Na4XeO6↓+Xe↑+O2↑+12F﹣
+8H2O
下列说法错误的是( )
A.XeO3具有平面三角形结构
B.OH﹣的还原性比 H2O强
C.反应 i~iv 中有 3个氧化还原反应
D.反应 iv 每生成 1mol O2,转移6mol 电子
3.(2024•浙江)利用 CH3OH 可将废水中的 转化为对环境无害的物质后排放。反应原理为:H+
+CH3OH+ →X+CO2+H2O(未配平)。下列说法正确的是( )
A.X表示NO2
B.可用 O3替换 CH3OH
C.氧化剂与还原剂物质的量之比为6:5
D.若生成标准状况下的 CO2气体11.2L,则反应转移的电子数为2NA(NA表示阿伏加德罗常数的值)
4. ( 2024• 浙 江 )汽 车 尾 气 中 的 NO 和CO 在催化 剂 作 用下 发 生 反 应 : 2NO+2CO
2CO2+N2,下列说法不正确的是( )(NA为阿伏加德罗常数的值)
A.生成 1molCO2转移电子的数目为2NA
B.催化剂降低 NO 与CO 反应的活化能
C.NO 是氧化剂,CO 是还原剂
D.N2既是氧化产物又是还原产物
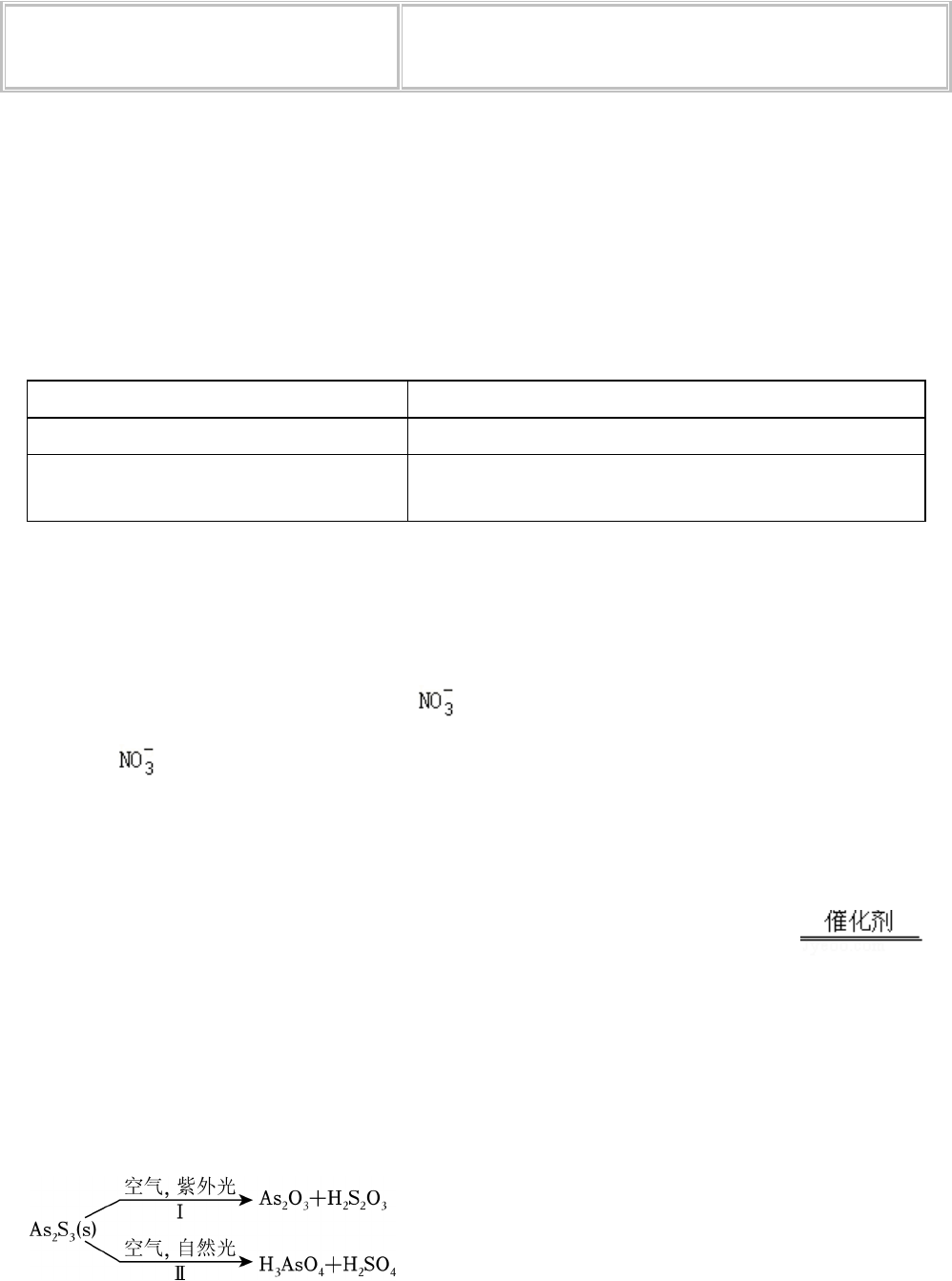
5.(2023•湖南)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜
料雌黄(As2S3)褪色的主要原因是发生了以下两种化学反应:
第2页(共 24 页)






