第1章 第2讲 离子反应 离子方程式---2025年高考化学一轮复习(新高考)
1
第2讲 离子反应 离子方程式
复习目标 1.了解电解质及其分类,掌握强弱电解质的本质区别。2.理解电解质在水溶液
中的电离以及电解质溶液的导电性。3.了解离子反应的概念、离子反应发生的条件,并能正
确书写离子方程式。
考点一 电解质及电离
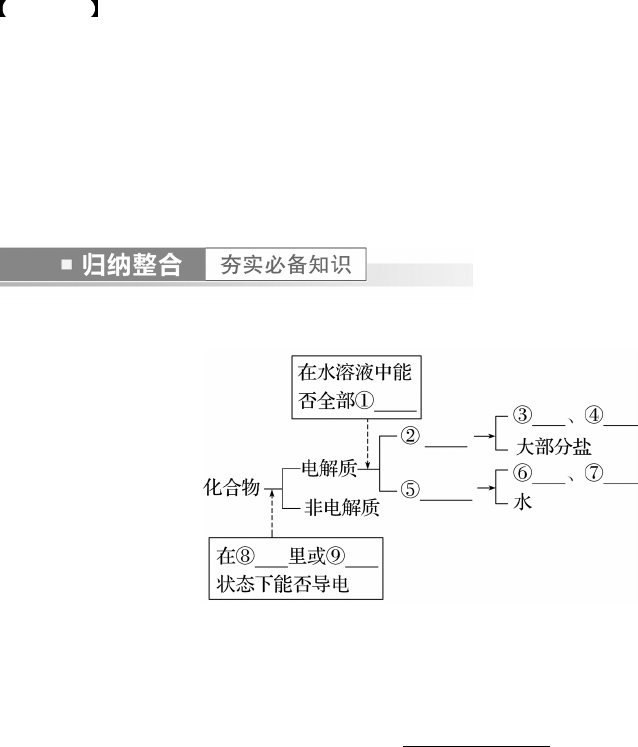
1.电解质及其分类
答案 ①电离 ②强电解质 ③强酸 ④强碱 ⑤弱电解质 ⑥弱酸 ⑦弱碱 ⑧水溶液
⑨熔融
2.电解质的电离
(1)电离:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
(2)电离方程式:用化学式和离子符号表示电解质溶于水或熔融状态下电离成离子的式子。
3.电离方程式的书写方法
(1)强电解质的电离方程式中用“===”连接。
按要求书写下列电解质的电离方程式:
①Ba(OH)2:___________________________________________________;
②KAl(SO4)2:__________________________________________________;
③NaHSO4溶于水:______________________________________________;
④NaHSO4熔融:________________________________________________。
答案 ① Ba(OH)2===Ba2++2OH-
②KAl(SO4)2===K++Al3++2SO
③NaHSO4===Na++H++SO
④NaHSO4===Na++HSO

2
(2)弱电解质的电离方程式中用“”连接。
多元弱酸,分步电离,分步书写,且第一步的电离程度远大于第二步的电离程度;多元弱碱,
分步电离,一步书写;弱酸的酸式盐,“强中有弱”。
按要求书写电离方程式:
①CH3COOH:______________________________________________________。
②H2CO3:__________________________________________________________。
③Fe(OH)3:_________________________________________________________。
④NaHCO3:_________________________________________________________。
答案 ① CH3COOHCH3COO-+H+
②H2CO3H++HCO、HCOH++CO ③ Fe(OH)3Fe3++3OH-
④NaHCO3===Na++HCO、HCOH++CO
1.CO2、NH3溶于水能导电,所以二者为电解质( )
2.NaCl 溶液在电流的作用下电离成钠离子和氯离子( )
3.强电解质都是离子化合物,弱电解质都为共价化合物( )
4.BaSO4的水溶液不易导电,但 BaSO4是强电解质( )
5.HClO 是弱酸,但 NaClO 是强电解质( )
答案 1.× 2.× 3.× 4.√ 5.√
一、电解质、非电解质、强弱电解质的判断
1.现有 12 种物质:① Al ②稀硝酸 ③ HNO3 ④ NH3·H2O ⑤ CO2 ⑥空气 ⑦ NaCl
⑧CaCO3 ⑨NaHCO3 ⑩乙醇 ⑪Al2O3 ⑫Cu(OH)2
按照表中提示的信息,把符合左栏条件的物质的序号填入右栏相应的位置。
序号 符合的条件 物质的序号
(1) 混合物
(2) 强电解质,但熔融状态下并不导电
(3) 电解质,熔融状态下能导电
(4) 强电解质,但难溶于水
(5) 非电解质
(6) 既不是电解质,也不是非电解质,但本身能导电
(7) 弱电解质
答案 (1)②⑥ (2)③ (3)⑦⑧⑨⑪⑫ (4)⑧⑪ (5)⑤⑩ (6)①② (7)④⑫
二、离子反应过程中溶液导电性变化的判断






